Nosokomial lungebetændelse er den mest almindelige og alvorlige nosokomielle infektion, hvoraf ventilatorassocieret lungebetændelse (VAP) tegner sig for 40%. VAP forårsaget af refraktære patogener er stadig et vanskeligt klinisk problem. I årevis har retningslinjer anbefalet en række interventioner (såsom målrettet sedation, hovedløft) for at forebygge VAP, men VAP forekommer hos op til 40% af patienter med trakeal intubation, hvilket resulterer i længere hospitalsophold, øget brug af antibiotika og død. Folk leder altid efter mere effektive forebyggende foranstaltninger.
Ventilatorassocieret lungebetændelse (VAP) er en ny type lungebetændelse, der udvikler sig 48 timer efter trakeal intubation og er den mest almindelige og dødelige nosokomielle infektion på intensiv afdeling (ICU). Retningslinjerne fra American Society of Infectious Diseases fra 2016 har adskilt VAP fra definitionen af hospitalserhvervet lungebetændelse (HAP) (HAP refererer kun til lungebetændelse, der opstår efter indlæggelse uden trakealtub og ikke er relateret til mekanisk ventilation; VAP er lungebetændelse efter trakeal intubation og mekanisk ventilation), og European Society og Kina mener, at VAP stadig er en særlig type HAP [1-3].
Hos patienter, der modtager mekanisk ventilation, varierer forekomsten af VAP fra 9% til 27%, dødeligheden anslås til 13%, og det kan føre til øget systemisk antibiotikaforbrug, forlænget mekanisk ventilation, forlænget ophold på intensivafdelingen og øgede omkostninger [4-6]. HAP/VAP hos ikke-immunsvage patienter er normalt forårsaget af bakteriel infektion, og fordelingen af almindelige patogener og deres resistenskarakteristika varierer med region, hospitalsklasse, patientpopulation og antibiotikaeksponering og ændrer sig over tid. Pseudomonas aeruginosa dominerede VAP-relaterede patogener i Europa og Amerika, mens flere Acinetobacter baumannii blev isoleret på tertiære hospitaler i Kina. En tredjedel til halvdelen af alle VAP-relaterede dødsfald er direkte forårsaget af infektionen, hvor dødeligheden for tilfælde forårsaget af Pseudomonas aeruginosa og acinetobacter er højere [7,8].
På grund af den stærke heterogenitet af VAP er den diagnostiske specificitet af dens kliniske manifestationer, billeddiagnostik og laboratorietests lav, og differentialdiagnoserne er brede, hvilket gør det vanskeligt at diagnosticere VAP i tide. Samtidig udgør bakteriel resistens en alvorlig udfordring for behandlingen af VAP. Det anslås, at risikoen for at udvikle VAP er 3%/dag i løbet af de første 5 dage med brug af mekanisk ventilation, 2%/dag mellem 5 og 10 dage og 1%/dag i resten af tiden. Den maksimale incidens forekommer generelt efter 7 dages ventilation, så der er et vindue, hvor infektion kan forebygges tidligt [9,10]. Mange undersøgelser har set på forebyggelse af VAP, men på trods af årtiers forskning og forsøg på at forebygge VAP (såsom at undgå intubation, forhindre reintubation, reducere sedation, hæve hovedgærdet med 30° til 45° og mundpleje) ser incidensen ikke ud til at være faldet, og den tilhørende medicinske byrde er fortsat meget høj.
Inhalerede antibiotika er blevet brugt til behandling af kroniske luftvejsinfektioner siden 1940'erne. Fordi det kan maksimere tilførslen af lægemidler til infektionsmålet (dvs. luftvejene) og reducere systemiske bivirkninger, har det vist god anvendelsesværdi i en række forskellige sygdomme. Inhalerede antibiotika er nu godkendt af den amerikanske fødevare- og lægemiddelstyrelse (FDA) og det europæiske lægemiddelagentur (EMA) til brug ved cystisk fibrose. Inhalerede antibiotika kan reducere bakteriemængden og hyppigheden af eksacerbationer i bronkiektasi betydeligt uden at øge de samlede bivirkninger, og nuværende retningslinjer har anerkendt dem som førstelinjebehandling for patienter med pseudomonas aeruginosa-infektion og hyppige eksacerbationer. Inhalerede antibiotika i den perioperative periode efter lungetransplantation kan også bruges som adjuverende eller profylaktiske lægemidler [11,12]. Men i de amerikanske VAP-retningslinjer fra 2016 manglede eksperterne tillid til effektiviteten af adjuverende inhalerede antibiotika på grund af manglen på store randomiserede kontrollerede forsøg. Fase 3-forsøget (INHALE), der blev offentliggjort i 2020, gav heller ikke positive resultater (inhalation af amikacin-assisteret intravenøs antibiotika til behandling af gramnegativ bakterieinfektion forårsaget af VAP-patienter, et dobbeltblindet, randomiseret, placebokontrolleret fase 3-effektforsøg, i alt 807 patienter, systemisk medicinering + assisteret inhalation af amikacin i 10 dage).
I denne sammenhæng anvendte et team ledet af forskere fra det regionale universitetshospital i Tours (CHRU) i Frankrig en anden forskningsstrategi og gennemførte et investigatorinitieret, multicenter, dobbeltblindet, randomiseret kontrolleret effektforsøg (AMIKINHAL). Inhaleret amikacin eller placebo til forebyggelse af VAP blev sammenlignet i 19 patienter i Frankrig [13].
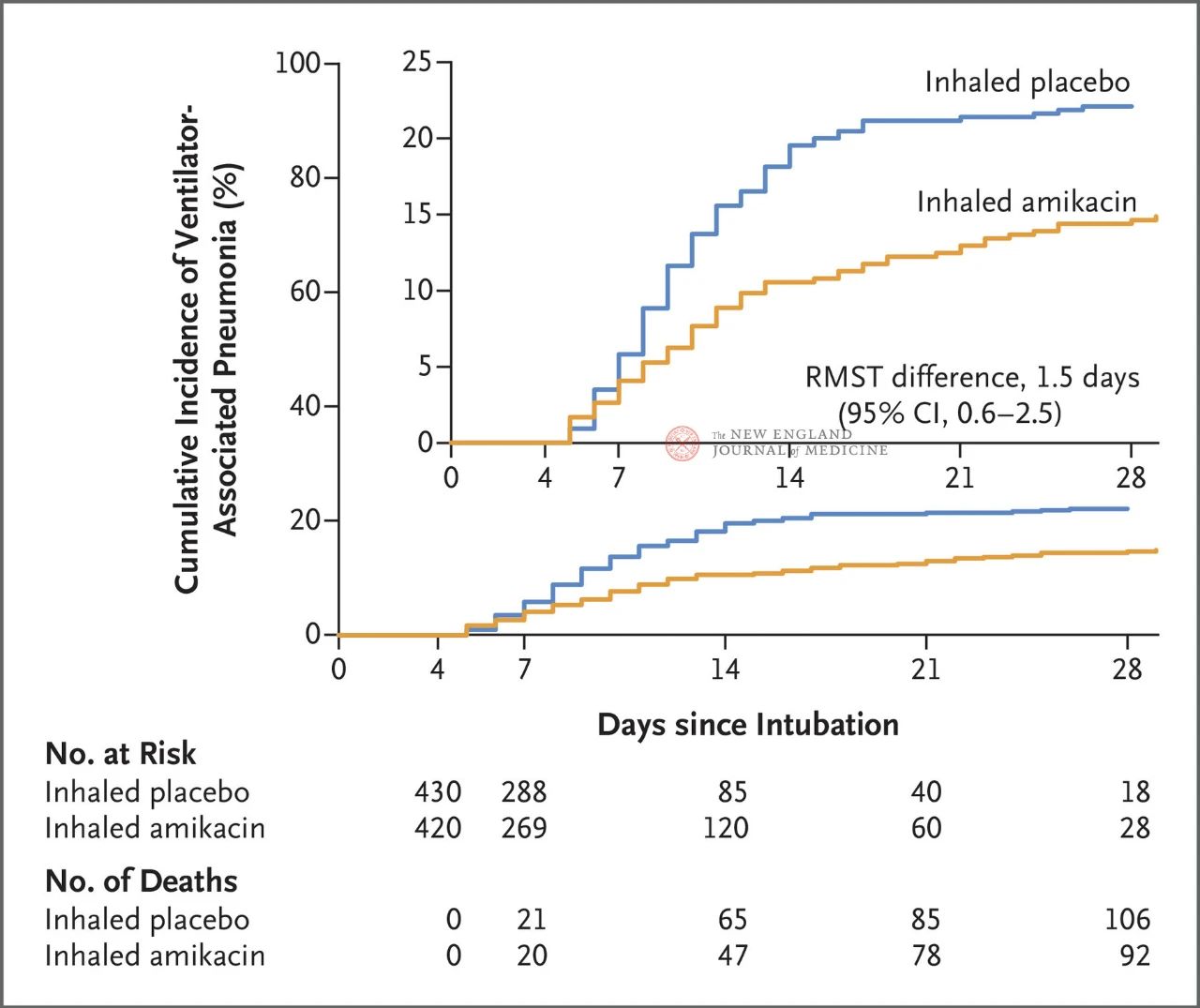
I alt 847 voksne patienter med invasiv mekanisk ventilation mellem 72 og 96 timer blev tilfældigt tildelt 1:1 til inhalation af amikacin (N = 417,20 mg/kg ideel kropsvægt, QD) eller inhalation af placebo (N = 430, 0,9% natriumkloridækvivalent) i 3 dage. Det primære endepunkt var den første episode af invasiv mekanisk ventilation fra begyndelsen af den randomiserede tildeling til dag 28.
Resultaterne af forsøget viste, at efter 28 dage havde 62 patienter (15%) i amikacin-gruppen udviklet VAP, og 95 patienter (22%) i placebogruppen havde udviklet VAP (den begrænsede gennemsnitlige overlevelsesforskel for VAP var 1,5 dage; 95% CI, 0,6~2,5; P=0,004).
Med hensyn til sikkerhed oplevede syv patienter (1,7%) i amikacingruppen og fire patienter (0,9%) i placebogruppen alvorlige bivirkninger relateret til forsøget. Blandt dem, der ikke havde akut nyreskade ved randomisering, havde 11 patienter (4%) i amikacingruppen og 24 patienter (8%) i placebogruppen akut nyreskade på dag 28 (HR, 0,47; 95% CI, 0,23~0,96).
Det kliniske forsøg havde tre højdepunkter. For det første trækker AMIKINHAL-forsøget, hvad angår studiedesign, på IASIS-forsøget (et randomiseret, dobbeltblindet, placebokontrolleret, parallelt fase 2-forsøg med 143 patienter). For at evaluere sikkerheden og effektiviteten af amikacin-fosfomycin inhalation systemisk behandling af gramnegativ bakterieinfektion forårsaget af inhalationsantibiotika (VAP) og INHALE-forsøget med negative resultater, er der opnået erfaringer, der fokuserer på forebyggelse af VAP, og relativt gode resultater. På grund af karakteristikaene ved høj dødelighed og langt hospitalsophold hos patienter med mekanisk ventilation og VAP, vil det være mere værdifuldt for klinisk praksis, hvis amikacin inhalation kan opnå signifikant forskellige resultater med hensyn til at reducere død og hospitalsophold hos disse patienter. I betragtning af heterogeniteten i sen behandling og pleje hos hver patient og hvert center er der dog en række forstyrrende faktorer, der kan forstyrre studiet, så det kan også være vanskeligt at opnå et positivt resultat, der kan tilskrives inhalerede antibiotika. Derfor kræver et vellykket klinisk studie ikke kun fremragende studiedesign, men også valg af passende primære endepunkter.
For det andet, selvom aminoglykosidantibiotika ikke anbefales som et enkelt lægemiddel i forskellige VAP-retningslinjer, kan aminoglykosidantibiotika dække almindelige patogener hos VAP-patienter (herunder pseudomonas aeruginosa, acinetobacter osv.), og på grund af deres begrænsede absorption i lungeepitelceller, høje koncentration på infektionsstedet og lave systemiske toksicitet. Aminoglykosidantibiotika er bredt foretrukket blandt inhalerede antibiotika. Denne artikel er i overensstemmelse med det omfattende estimat af effektstørrelsen af intratrakeal administration af gentamicin i små prøver, der tidligere er offentliggjort, hvilket tilsammen demonstrerer effekten af inhalerede aminoglykosidantibiotika i forebyggelsen af VAP. Det skal også bemærkes, at de fleste af de placebokontroller, der blev udvalgt i forsøgene relateret til inhalerede antibiotika, er normal saltvand. I betragtning af at forstøvet inhalation af normal saltvand i sig selv kan spille en vis rolle i fortynding af sputum og hjælpe med slimløsende midler, kan normal saltvand imidlertid forårsage en vis interferens i analysen af studieresultaterne, hvilket bør overvejes grundigt i undersøgelsen.
Derudover er lokal tilpasning af HAP/VAP-medicinering vigtig, ligesom antibiotikaprofylakse. Samtidig er økologien på den lokale intensivafdeling, uanset intubationstidens længde, den vigtigste risikofaktor for infektion med multiresistente bakterier. Derfor bør den empiriske behandling så meget som muligt referere til de mikrobiologiske data fra lokale hospitaler og kan ikke blindt referere til retningslinjer eller erfaringer fra tertiære hospitaler. Samtidig er kritisk syge patienter, der kræver mekanisk ventilation, ofte kombineret med multisystemsygdomme, og under den kombinerede påvirkning af flere faktorer, såsom stresstilstand, kan der også være et fænomen med krydstale mellem tarmmikrober og lungerne. Den høje heterogenitet af sygdomme forårsaget af intern og ekstern superposition bestemmer også, at den omfattende kliniske promovering af hver ny intervention er lang vej endnu.
Opslagstidspunkt: 2. dec. 2023