Blandet hyperlipidæmi er karakteriseret ved forhøjede plasmaniveauer af lavdensitetslipoproteiner (LDL) og triglyceridrige lipoproteiner, hvilket fører til en øget risiko for aterosklerotisk hjerte-kar-sygdom hos denne patientpopulation.
ANGPTL3 hæmmer lipoproteinlipase og endosepiase, samt leverens optagelse af triglyceridrige lipoproteiner. Bærere af den ANGPTL3-inaktiverede variant havde lavere niveauer af triglycerider, LDL-kolesterol, high-density lipoprotein (HDL)-kolesterol og ikke-HDL-kolesterol, samt en lavere risiko for aterosklerotisk hjerte-kar-sygdom. zodasiran er et lille interfererende RNA (RNAi)-lægemiddel, der er rettet mod ANGPTL3-ekspression i leveren.
Blandet hyperlipidæmi refererer til forhøjede niveauer af lipoprotein-kolesterol med lav densitet (LDL-C) og triglyceridrige lipoproteiner. Triglyceridrige lipoproteiner (herunder chylomikroner, lipoproteiner med meget lav densitet (VLDL) og restkolesterol) spiller en vigtig rolle i udviklingen af aterosklerotisk sygdom. Der findes ingen effektiv behandling for blandet hyperlipidæmi.
Bates er kendt for at reducere triglycerid (TG) niveauer, men reduktionen er begrænset. Samtidig har TG-sænkende lægemidler, herunder Bates (såsom eicosapentaeneddikesyre osv.), ingen signifikant effekt på risikoen for åreforkalkning forårsaget af forhøjede restkolesterolniveauer. Derudover har tidligere undersøgelser af patienter, der allerede tager statiner, vist, at kombinations-TG-sænkende lægemidler ikke reducerer risikoen for kardiovaskulære hændelser. Disse faktorer gør behandlingen af blandet hyperlipidæmi meget vanskelig.
ANGPTL3 (angiopoietin-lignende protein 3) regulerer lipider og lipoproteinmetabolisme, herunder TG og ikke-højdensitetslipoproteinkolesterol (HDL-C), ved reversibelt at hæmme lipoproteinlipase, endosepiase og lavdensitetslipoprotein (LDL)-receptorafhængig hepatisk lipoproteinoptagelse. Det har vist sig, at ANGPTL3-inaktiveringsvarianten fører til øget lipoproteinlipase- og endosepiaseaktivitet, hvilket igen fører til lave plasmalipoproteinniveauer i de fleste tilfælde. Disse omfatter triglyceridrige lipoproteiner (dvs. chylomikroner, restkolesterol, VLDL, mediumdensity lipoprotein [IDL]), LDL, højdensitetslipoprotein (HDL), lipoprotein (a) og deres kolesterolkomponenter. Heterozygote personer, der bærer denne variant, har en cirka 40% reduceret risiko for aterosklerotisk sygdom, og der er ikke fundet nogen negativ klinisk fænotype. ANGPTL3 udtrykkes i leveren, og gensilencingbehandlinger, der er målrettet mod dets mRNA, kendt som small interfering RNA (siRNA)-lægemidler, er en lovende hybridbehandling for hyperlipidæmi.
Den 12. september 2024 offentliggjorde New England Journal of Medicine (NEJM) et ARCHES 2-studie, der bekræftede, at siRNA-lægemidlet zodasiran signifikant reducerede TG-niveauer hos patienter med blandet hyperlipidæmi [1]. ARCHES-2 er et dobbeltblindet, placebokontrolleret fase 2b-studie med fokus på dosisintervaludforskning. I alt 204 patienter med blandet hyperlipidæmi (fastende TG-niveauer 150-499 mg/dl, LDL-C-niveauer ³70 mg/dl eller ikke-HDL-C-niveauer ³100 mg/dl) blev inkluderet. De blev opdelt i en zodasiran 50 mg-gruppe, en 100 mg-gruppe, en 200 mg-gruppe og en placebokontrolgruppe. Patienterne modtog subkutane injektioner i uge 1 og 12 og modtog opfølgende profylakse indtil uge 36.
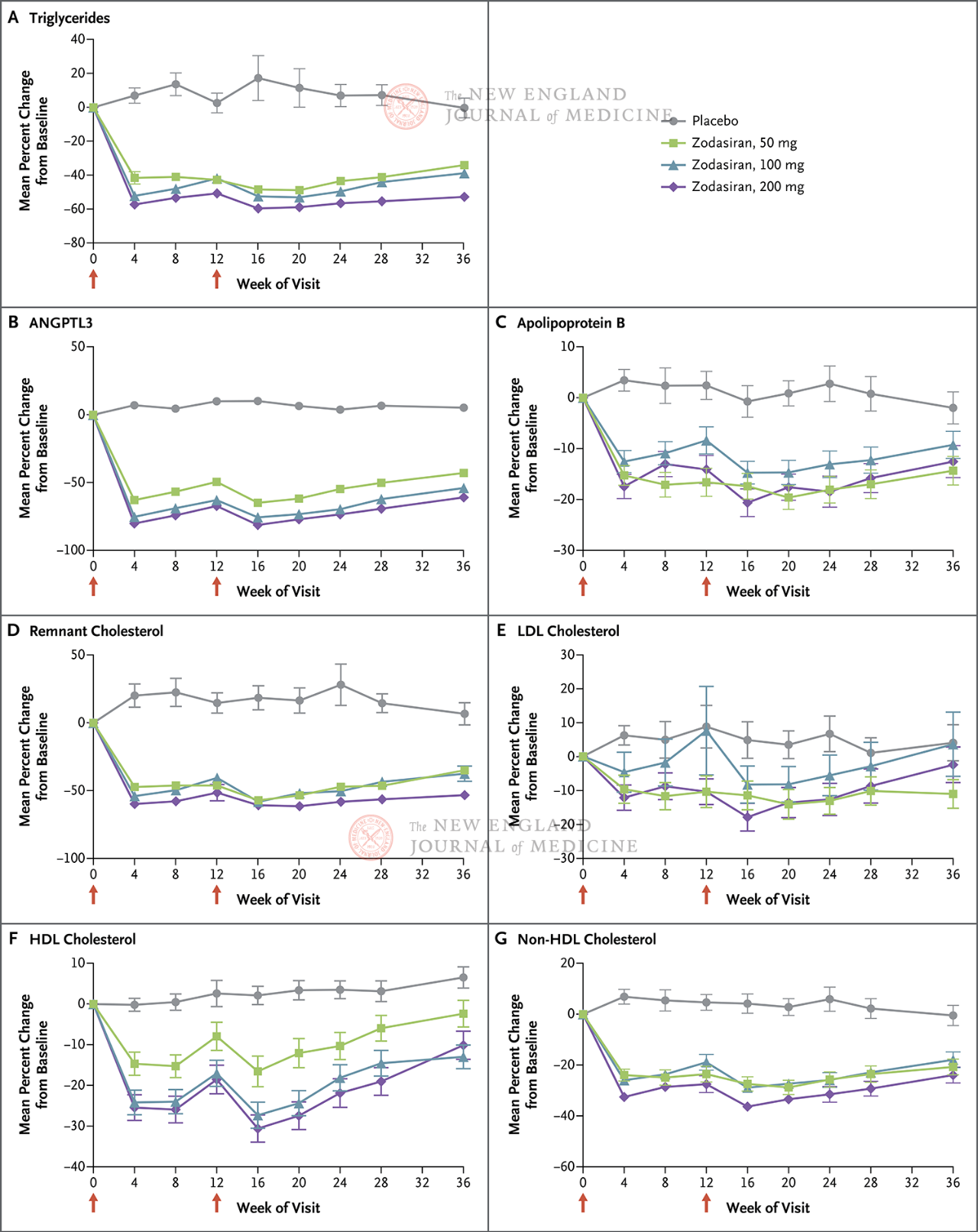
Det primære endepunkt var den procentvise ændring i TG fra baseline til uge 24. Undersøgelsen viste, at TG-niveauerne i zodasiran-gruppen var signifikant reduceret dosisafhængigt i uge 24 (TG-niveauerne i hver dosisgruppe var reduceret med henholdsvis 51, 57 og 63 procentpoint sammenlignet med placebogruppen) (P < 0,001 for alle sammenligninger). ANGPTL3 faldt også med henholdsvis 54 procentpoint, 70 procentpoint og 74 procentpoint. Ikke-HDL-c-niveauer faldt med 29 procentpoint, 29 procentpoint og 36 procentpoint, apolipoprotein B-niveauer faldt med 19 procentpoint, 15 procentpoint og 22 procentpoint, og LDL-C-niveauer faldt med henholdsvis 16 procentpoint, 14 procentpoint og 20 procentpoint, og disse resultater varede indtil den 36. uge. I uge 24 var zodasiran
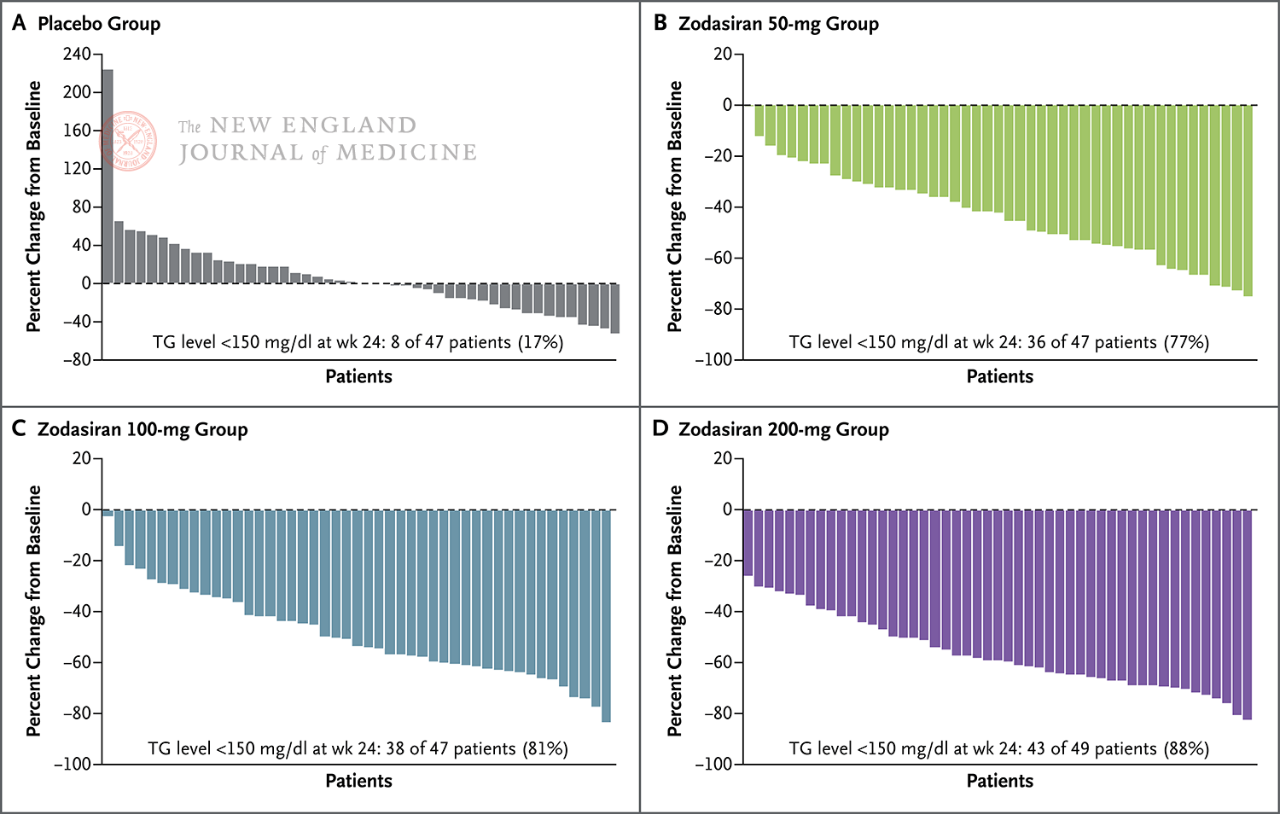
Hos 88 % af patienterne i 200 mg-gruppen var fastende triglycerider faldet til normalområdet.
Røde pile på dag 1 og 12 angiver administration af zodasiran eller placebo.
Fastende TG-niveauer faldt til normalt i uge 24 (150
mg/dl eller mindre)
Hver søjle repræsenterer én patient.
Studiet observerede også, at zotasiran var sikkert i alle dosisgrupper, hvor kun 2 patienter afbrød studiet på grund af bivirkninger (1 i placebogruppen og 1 i 100 mg zotasiran-gruppen). Alle alvorlige bivirkninger i zotasiran-gruppen forsvandt ved studiets afslutning, og der var ét dødsfald i placebogruppen. Den eneste bivirkning, der gav anledning til bekymring, var en stigning i HBA1c i 200 mg zotasiran-gruppen sammenlignet med placebo (gennemsnitlig ændring fra baseline til uge 24 [±SD], 0,38 ± 0,66 % vs. -0,03 ± 0,88 % hos patienter med præeksisterende diabetes). Patienter uden diabetes var 0,12 ± 0,19 % vs. -0,03 ± 0,19 %).
Især blev næsten alle patienter i studiet (96%) behandlet med statiner (hvoraf 37% var højdosisstatiner), 1% blev behandlet med en proproteinkonverterende enzym-subtilysin 9-hæmmer (PCSK9i), og 21% blev behandlet med fibrater. Derfor opnåede tilføjelse af zodasiran på basis af den nuværende konventionelle behandlingsregime stadig betydelige lipidsænkende effekter, hvilket giver et nyt regime til behandling af blandet hyperlipidæmi i fremtiden.
I uge 24 reducerede den maksimale dosis på 200 mg zotasiran i studiet restkolesterolniveauet med 34,4 mg/dl sammenlignet med placebo. Baseret på nuværende modeller forventes denne reduktion at reducere større kardiale bivirkninger med 20 procent. Zodasiran har potentiale til at blive brugt som monoterapi for alle lipoproteinkomponenter for at reducere risikoen for kardiovaskulære hændelser hos patienter. Yderligere forskning er derfor nødvendig for at bestemme dette lægemiddels potentiale til at reducere risikoen for åreforkalkning.
Fase 2b-studiet, dobbeltblindet, randomiseret, placebokontrolleret MUIR, som blev offentliggjort samtidigt i NEJM, anvendte et andet siRNA-lægemiddel, plozasiran, til behandling af blandet hyperlipidæmi [2]. plozasiran er designet til at reducere ekspressionen af APOC3, genet der koder for apolipoprotein C3 (APOC3), en regulator af TG-metabolisme, i leveren, hvorved TG og restkolesterolniveauer reduceres. Reduktionerne i TG og restkolesterolniveauer observeret i studiet var tilsvarende dem, der blev fundet i ARCHES-2-studiet. Derfor spekuleres det i, at de to lægemidler hos patienter med blandet hyperlipidæmi har lignende virkninger på at reducere niveauet af triglyceridrigt lipoprotein og restkolesterol.
Resultaterne af de to siRNA-studier viser, at dette er en meget lovende klasse af lægemidler, der vil bringe nye muligheder for behandling af blandet hyperlipidæmi og forbedre kardiovaskulære resultater hos patienter.
Opslagstidspunkt: 15. september 2024